随着我*经济的高速发展, 工矿企业产生的废
水呈现出高浓度
〔1〕、难生物降解
〔2〕和水质复杂
〔3〕等特点, 传统的生化处理方法已很难达到相应的排放标准要求。 近十几年兴起的**氧化技术能高效降解污染物或提高废水的可生化性
〔4〕,因而受到人们的关注。 其中,活化氧化剂(H
2O
2、O
3 等)产生羟基自由
基(·OH),活化过硫酸盐产生硫酸根自由基(SO·
-)
4
的作用机理成为当前研究的热点。
COD 可反映废水中有机物的相对含量,还原性无机物质对 COD 的测定有影响。 废水体系中残留的无机活化物质
〔5〕会导致 COD 测定值偏高或混淆滴定终点。过硫酸盐作为一种氧化性物质,在遇到氧化性更强的物质如重铬酸钾时则充当还原剂。 因此在
COD 测定过程中,残留的过硫酸盐作为还原性物质与重铬酸钾反应,会引起 COD 测定误差。 若加入掩蔽剂如高锰酸钾、 硫代硫酸钠和亚硫酸钾等可以消除其干扰,但剩余的掩蔽剂又形成新的干扰。 因此,寻找一种简单、快速、可靠的方法来消除过硫酸盐以
准确测定 COD 是十分必要的。 笔者考察了过硫酸盐
(过硫酸钾)对 COD 测定的干扰,分析产生干扰的原因,并提出消除干扰的措施,为准确测定废水 COD
提供依据。
1 实验部分
1.1 主要仪器与试剂
仪 器:DR200 型
消解器(美* HACH 公司),带
聚四氟乙烯盖的消解管(50 mL),N/C2100 型 TOC
分析仪(德*耶拿公司),MIC 型离子色谱仪(瑞士万通公司)。 试剂:按 HZ-HJ-SZ-0108《水质化学需氧量的测定 密封催化消解法》、GB/T 641—1994《化学试剂 过二硫酸钾(过硫酸钾)》中试剂使用和配制要求执行。
1.2 测定方法
COD 按 HZ-HJ-SZ-0108 进行测定。
K
2S
2O
8 参照 GB/T 641—1994 中硫代硫酸钠滴定法测定, 原理:K
2S
2O
8 在酸性溶液中具有强氧化性,可将碘离子氧化成碘单质。 吸取 5 mL 稀释过的
K
2S
2O
8 溶液放入 150 mL 干燥碘量瓶中,加入 30 mL
水、1 g 碘化钾, 摇匀, 在暗处放置 30 min。 加入
2 mL 乙酸(体积分数 36%),用硫代硫酸钠标准溶液
(0.05 mol/L)滴定。 近终点时,加入 2 mL 淀粉指示液(10 g/L),继续滴定**溶液蓝色消失,同时作空白实验和原水样背景实验。 反应式如下:
S
2O
82-+2I
-=I
2+2SO
42- (1)
2S
2O
32-+I
2=S
4O
62-+2I
- (2)
上述方法适用于测定过程中不产生硫酸根自由基的待测水样。 若待测水样中可能存在能将碘离子氧化成碘单质的其他物质, 用硫代硫酸钠滴定法测定 K
2S
2O
8 可能会造成测定值高于实际值。 硫酸根自由基与其他物质反应生成 SO
42-,采用离子色谱法测定待测水样中的 SO
42-浓度, 可间接得到剩余 K
2S
2O
8
浓度,同时须扣除原水样中 SO
42-背景浓度。
2 结果与讨论
2.1 K
2S
2O
8 质量浓度与 COD 的关系
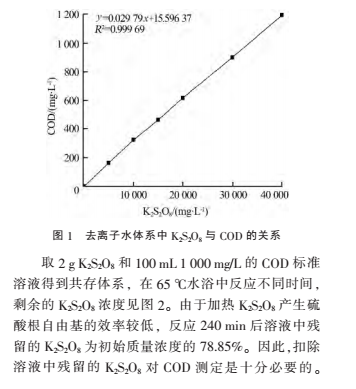
用去离子水配制不同质量浓度的 K
2S
2O
8 溶液,测定其对应的 COD,结果如图 1 所示。 显然,K
2S
2O
8质量浓度与 COD 之间呈现显著的线性关系,得到线性方程为:y=0.029 79x+15.596 37,R
2 为 0.999 69。
结合图 1 分析,1 mg K
2S
2O
8 对 COD 变化值的贡
献为 0.029 79 mg。
2.1 水样中K
2S
2O
8 对 COD 变化值的贡献
在 去离子水体系中 K
2S
2O
8 质量浓度与其造成的 COD 变化量呈显著的正相关关系。而 K
2S
2O
8 虽比
较稳定,但在高温条件下能分解产生硫酸根自由基,
或与水中的还原性物质发生化学反应。 且实际废水体系成分复杂, 与 K
2S
2O
8 之间的反应更为复杂,因此需考察 K
2S
2O
8 质量浓度与 COD 的对应关系在成分复杂的水样中是否依然成立, 来决定 2.1 的线性方程是否能用于分析实际水样。 分别选取 COD 标准溶液体系、 经生化处理后的垃圾渗滤液体系作为研究对象, 投加不同剂量的 K
2S
2O
8, 测定水样中残留 K
2S
2O
8 质量浓度及其 COD,借此分析残留 K
2S
2O
8 对实际水样 COD 测定结果的影响。
(1)COD 标准溶液体系。 在 50 mL COD 标准溶液中( 理论 COD 为 1 000 mg/L) 投加不同剂量的K
2S
2O
8,测定其 COD,结果见表 1。 在 COD 标准溶液体系中,K
2S
2O
8 的引入导致溶液 COD 相应的升高。由表 1 回收率可知,在消解(165 ℃)之前,K
2S
2O
8 和重铬酸钾通过反应消耗完全。 因此在消解过程中不会出现 K
2S
2O
8 产生硫酸根自由基降解 COD 标准溶
|
液从而影响测定结果的情况 |
|
|
|
|
|
|
。 |
|
|
|
|
|
|
2- 加热 |
- |
(3) |
|
|
|
S2O8 →2SO4· |
|
表 1 |
加入 K2S2O8 后 COD 标准溶液的 COD |
|
K2S2O8 质量浓 加标量/ |
测定值/ |
加标后理论 |
回收 |
|
|
度/(mg·L-1) |
(mg·L-1) |
(mg·L-1) |
值/(mg·L-1) |
率/% |
|
5 000 |
1 000 |
1 144.68 |
1 148.15 |
99.69 |
|
|
10 000 |
1 000 |
1 295.88 |
1 296.30 |
99.96 |
|
|
15 000 |
1 000 |
1 446.97 |
1 444.45 |
100.17 |
|
|
20 000 |
1 000 |
1 600.43 |
1 592.60 |
100.49 |
|
|
30 000 |
1 000 |
1 900.53 |
1 888.90 |
100.62 |
|
|
40 000 |
1 000 |
2 190.05 |
2 185.20 |
100.22 |
|
设含 K
2S
2O
8 的 COD 标准溶液 COD 为 c
1,COD标准溶液的 COD 为 c
0, COD
1=c
1-c
0; 通过 2.1 线性
|
方程计算 K2S2O8 |
对 COD 变化值的贡献为 |
COD2。 |
|
在 COD 标准溶液体系中对 |
|
COD1、 COD2 |
进行比 |
|
较,结果见图 3。 |
由图 3 发现 COD1 |
与 COD2 差值 |
|
较小 |
约为 |
8.76~19.87 mg/L, |
为 |
COD |
标准溶液 |
COD |
|
|
|
, |
|
|
|
|
|
|
的 |
0.88%~1.99% |
。 |
由此说明在 |
COD |
标准溶液体系 |
|
|
|
|
|
|
|
|
|
中 |
, |
该线性方程能较好地反映 |
COD |
的实际差异 |
。 |
|
|
|
|
|
|
|
|
|
|
|
(2)垃圾渗滤液体系。在生化处理后的垃圾渗滤液体系中投加一定量的 K
2S
2O
8, 考察残留 K
2S
2O
8 引
起的 COD 变化情况。 由于垃圾渗滤液体系成分复杂,可能存在能与 K
2S
2O
8 反应的物质, 因此对反应 180 min 后垃圾渗滤液中剩余的 K
2S
2O
8 进行测定,结
果见表 2。 由表 2 可得,生化处理后的垃圾渗滤液体系中反应 180 min 后残留的 K
2S
2O
8 与实际投加K
2S
2O
8 **大差值为实际投加量的 6.56%, 说明在该体系中 K
2S
2O
8 没有明显分解。 K
2S
2O
8 一般在催化剂存在下才容易分解, 在常规条件下也不表现出较强的氧化性。 而在所有水样中测得的 K
2S
2O
8 都存在一定程度的降低, 可能是因为垃圾渗滤液中存在极少对 K
2S
2O
8 有催化作用的 Fe
2+等过渡金属离子, 与其发生反应产生硫酸根自由基
〔6〕:
|
|
n+ |
2- |
(n+1)+ |
- |
2- |
(4) |
|
|
Me +S2O8 =Me |
+ SO·4+SO4 |
|
表 2 |
渗滤液体系加入K2S2O8 前后的K2S2O8 质量浓度变化 |
|
|
|
|
|
|
|
|
|
|
|
项目 |
1 |
2 |
3 |
4 |
5 |
|
|
|
|
|
|
加入K2S2O8/(mg·L-1) |
40.0 |
60.0 |
90.0 |
120.0 |
150.0 |
|
|
3 h 后K2S2O8/(mg·L-1) |
37.8 |
56.6 |
84.1 |
113.9 |
142.2 |
|
注:垃圾渗滤液中可能存在能将碘离子氧化成碘单质的物质,因此该 K
2S
2O
8 质量浓度扣除空白实验的同时也应扣除垃圾渗滤液水样背景。
向垃圾渗滤液体系中投加不同剂量的 K
2S
2O
8 会导致体系的 COD 相应升高,结果见表 3。
|
表 3 |
投加 K2S2O8 后垃圾渗滤液体系的 COD |
|
K2S2O8 质量浓 渗滤液/ |
测定值/ |
加标后理论 |
回收 |
|
度/(mg·L-1) |
(mg·L-1) |
(mg·L-1) |
值/(mg·L-1) |
率/% |
|
5 000 |
535.26 |
680.49 |
683.41 |
99.57 |
|
10 000 |
535.26 |
825.99 |
831.51 |
99.33 |
|
15 000 |
535.26 |
972.10 |
979.71 |
99.22 |
|
20 000 |
535.26 |
1 140.06 |
1 127.86 |
101.08 |
|
30 000 |
535.26 |
1 414.52 |
1 424.16 |
99.32 |
|
40 000 |
535.26 |
1 703.99 |
1 720.46 |
99.04 |
设含 K
2S
2O
8 的垃圾渗滤液 COD 为 c
1,垃圾渗滤液的 COD 为 c
0, COD
1=c
1-c
0; 通过 2.1 线性方程计算 K
2S
2O
8 对 COD 变化值的贡献为 COD
2。 图 4 比较了垃圾渗滤液体系中 COD
1 与 COD
2, 发现
COD
1 与 COD
2 差异较小, 约为 6.60~38.47 mg/L,为垃圾渗滤液 COD 的 1.23%~7.18%。 说明在成分较
为复杂的垃圾渗滤液体系中,2.1 的线性方程也能较好地反映 COD 的实际差异。2.3 测定体系中 COD 与 TOC 的比较
TOC 表示水中总有机碳含量,是以碳量表征水
体中有机物质总量的综合指标,所有含碳物质如苯、吡啶等芳香烃类有毒有害物质均能反映在 TOC 指
标中。分别向 COD 标准溶液和垃圾渗滤液体系中加入不同剂量的 K
2S
2O
8,在 65 ℃水浴中反应 300 min,测定溶液的 COD 和 TOC,结果如图 5、图 6 所示。 在 65 ℃下过硫酸钾产生硫酸根自由基, 对 COD 标准
溶液降解效果较好,COD、TOC 的**高去除率分别为
97.49%、97.46%; 其对垃圾渗滤液的处理效果也较好,COD、TOC 的**高去除率达到 96.15%、95.33%。
通过对比不难发现, 由于残留的 K
2S
2O
8 对 COD 测定造成影响, 没有扣除 K
2S
2O
8 干扰的 COD 不能准确反映处理效果; 而扣除 K
2S
2O
8 干扰后的 COD 和 TOC 曲线符合理论处理效果,即随着 K
2S
2O
8 质量浓度的增加,去除率随之升高。
造成二次污染, 且测定时间较长。 而采用仪器分析
TOC,测样时间短 ,且目前很多 TOC 测定仪都采用自动进样系统,自动化程度较高。 由于 COD 表征的
是水体中的有机物和部分无机还原物质被氧化需要的氧化剂用量, 一定程度上不能排除无机还原物质的干扰。 因此对于标准样品或实际样品,测定 TOC 的精密度、准确度均比 COD 高;在测定有机污染物含量较低的水样时,COD 的测定结果误差较大。 鉴于 TOC 测定方法简单、准确且没有试剂污染,建议采用TOC 来代替 COD。
3 结论
(1)去离子水中 K
2S
2O
8 质量浓度与 COD 之间呈现显著的线性关系,1 mg K
2S
2O
8 对 COD 变化值的贡献为 0.029 79 mg。 将 K
2S
2O
8 加入 COD 标准溶液和垃圾渗滤液体系中会引起体系 COD 相应的升高。(2)通过计算得出 COD
1 和 COD
2 之间的差异,在生化处理后的垃圾渗滤液体系中其差值为 6.60~ 38.47 mg/L,为原渗滤液 COD 的 1.23%~7.18%。 说明
K
2S
2O
8质量浓度与 COD 之间的线性方程能较好地反映COD 的实际差异。 由线性方程 y=0.029 79x+ 15.596 37, 在测定 COD 前计算出 K
2S
2O
8 引起的
COD
2,可以消除其对 COD 测定引起的干扰。(3)测定水浴反应(65 ℃ ) 后 COD 标准溶液的 COD 和TOC, 扣除 K
2S
2O
8 干扰后的 COD 和 TOC 曲线均能较准确地反映处理效果。 由于 TOC 测定方法简单准确且没有试剂污染,更适于评价处理效果。
与 TOC 测定相比较,采用重铬酸钾法测定 COD
需使用 Ag
2SO
4 作为催化剂,若水样中含有较高的氯离子还需使用 HgSO
4 作掩蔽剂,这些试剂的使用易
